- 登入
- 註冊
猛健樂效果有限?女性平衡醫學解析:壓力性肥胖的真正源頭,是皮質醇與慢性發炎

撰文者:初悅婦研婦產科診所院長 婦產科專科 功能醫學 大象醫師 – 周維薪
- 妳有沒有過這種經驗:
- 聽說猛健樂效果驚人,咬牙自費打了三個月,前兩個月掉了三、四公斤,第三個月開始紋風不動。 身邊有人打了瘦十幾公斤,妳明明同樣認真,卻只瘦了一點點,停藥後甚至開始反彈。 然後妳開始懷疑 – 「是不是我體質不好?是不是我又失敗了?」
- 我想直接告訴妳:不是的。
很多時候不是猛健樂效果有限,而是它根本「打錯靶」。對於壓力性肥胖的女性來說,藥物在處理的是「食慾」,但妳真正的引擎,是一條完全不同的迴路 – 皮質醇與慢性發炎。
我們其實活在一個「壓力胖」被低估的時代
翻開現代職業女性的日常:早晨趕打卡、午餐配 deadline、回家還要顧訊息和家庭。睡眠不足、咖啡當水喝、情緒長期緊繃,這已經是 30 世代女性的生活底色。
而當減重議題被簡化成「熱量赤字」與「打針就會瘦」這種二元論時,真正高壓的女性反而是被誤解最深的一群。
她們不是不努力,而是身體的代謝設定,早就被慢性壓力悄悄改寫了。在「女性平衡醫學」的角度,這屬於代謝平衡(Metabolic Balance)的核心議題 – 而這也是猛健樂類藥物最容易踩空的地帶。
猛健樂作用的是「食慾」,不是「壓力」
猛健樂(Tirzepatide)是一種 GLP-1 / GIP 雙重受體促效劑,它的核心機轉是模擬腸道荷爾蒙,作用在大腦的飽食中樞,讓妳更早感到飽、更晚感到餓,同時延緩胃排空、提升胰島素敏感度。
對於「單純吃太多」型的肥胖,這條路徑非常有效 – 大型臨床試驗 SURMOUNT-1 顯示,Tirzepatide 最高劑量組 72 週可減重約 20.9%[1]。
但這條路徑有一個盲點:它幾乎不處理「壓力—皮質醇—內臟脂肪」這條軸線。
當一位女性的肥胖根源來自慢性壓力,她的身體並不是因為「吃太多」而胖,而是因為腎上腺持續分泌皮質醇,將熱量「指定」儲存到腰腹的內臟脂肪。這時,把食慾壓下來,就像在引擎仍全速運轉時拼命踩剎車 – 車是會慢下來,但脂肪依然非常難瘦下來。
更關鍵的是,SURMOUNT-4 研究指出,停用 Tirzepatide 後 52 週,患者平均反彈回原本減重幅度的一半以上[2]。對壓力源未處理的緊繃女性,這個反彈會更快、更明顯。
壓力性肥胖的真正引擎 – 腎上腺軸與皮質醇陷阱
讓我們一步一步看:
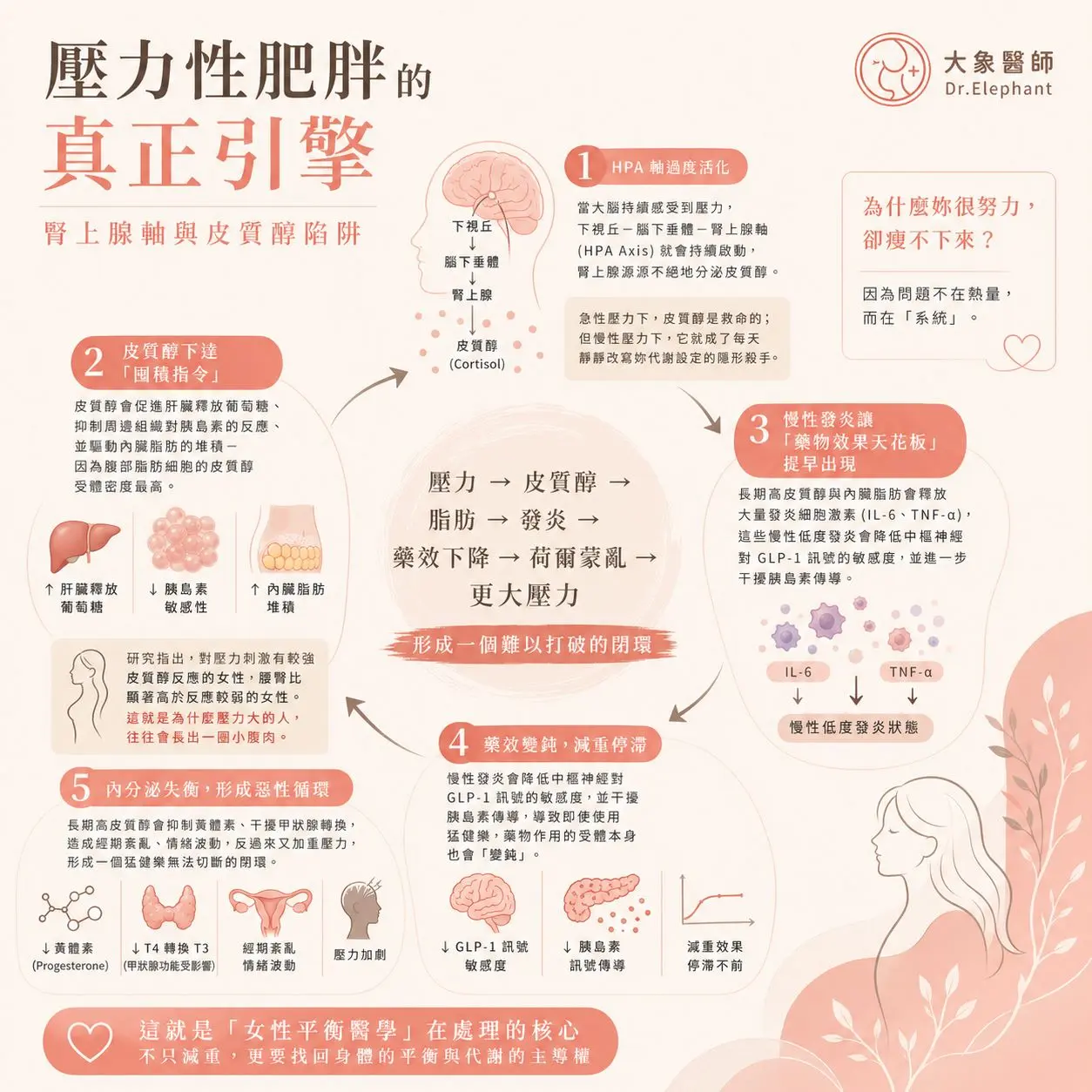
Step 1:HPA 軸過度活化
當大腦持續感受到壓力,下視丘—腦下垂體—腎上腺軸(HPA Axis)就會持續啟動,腎上腺源源不絕地分泌皮質醇[3]。
急性壓力下,皮質醇是救命的;但慢性壓力下,它就成了每天靜靜改寫妳代謝設定的隱形殺手。
Step 2:皮質醇下達「囤積指令」
皮質醇會促進肝臟釋放葡萄糖、抑制周邊組織對胰島素的反應、並驅動內臟脂肪的堆積 – 因為腹部脂肪細胞的皮質醇受體密度最高[4]。
研究明確指出,對壓力刺激有較強皮質醇反應的女性,腰臀比顯著高於反應較弱的女性[5]。這就是為什麼壓力大的人,往往會長出一圈小腹肉。
Step 3:慢性發炎讓「藥物效果天花板」提早出現
這一點最少人提,卻最是臨床上最關鍵的問題。
長期高皮質醇與內臟脂肪會釋放大量發炎細胞激素(IL-6、TNF-α),這些慢性低度發炎會降低中樞神經對 GLP-1 訊號的敏感度,並進一步干擾胰島素傳導[6]。
換句話說,當妳的身體處在慢性發炎狀態時,即使打了猛健樂,藥物作用的受體本身就會「變鈍」 – 這就是為什麼一樣的藥、一樣的劑量,高壓女性的減重曲線就是會比較平。
在「女性平衡醫學」的框架裡,這同時牽動了內分泌平衡:長期高皮質醇會抑制黃體素、干擾甲狀腺轉換,造成經期紊亂、情緒波動,反過來又加重壓力 – 形成一個猛健樂無法切斷的閉環。
妳有沒有發現,問題不在「神藥」夠不夠強?
很多女性以為,只要換更貴、更新的減重藥就能突破停滯。
但真正的關鍵是:當引擎還在燒,再好的剎車都只是短期效果。
藥物可以幫妳「降低吸收與食慾」,但它沒辦法幫妳 –
- 改善凌晨兩點還是翻來覆去的你的睡眠
- 關掉持續分泌壓力皮質醇的腎上腺
- 澆熄內臟脂肪所點燃的慢性發炎
所以不是猛健樂無效,而是對壓力性肥胖的女性,「先修復、再用藥」或「修復與藥物並進」,效果會比單獨用藥好得多。
對號入座:妳是不是壓力性肥胖的高風險族群?
在臨床上,我會留意以下訊號的組合:
代謝層面:體重增加集中在腰腹、空腹血糖偏高(100–125 mg/dL)、下午三、四點突發嗜睡與強烈食慾
內分泌層面:月經週期紊亂或 PMS 加劇、壓力期掉髮、晨起即使睡足仍無法恢復精神
睡眠與情緒層面:難以入睡或凌晨兩到四點醒來、腸躁症狀、對事物熱情下降
如果妳同時符合三項以上,這個組合本身就值得一次系統性的代謝平衡評估 – 而不是直接走進醫美診所打針。
如果需要藥物輔助 – 比起猛健樂,這兩類更貼近壓力性肥胖的機轉
如果評估後確實需要藥物介入,比起把目標放在「食慾抑制」,更值得納入考慮的是另外兩類藥物 – 它們的作用點,剛好打在猛健樂打不到的地方。
排糖藥(SGLT2 抑制劑):直接打擊「皮質醇的目標脂肪」
排糖藥(SGLT2i)原本用於糖尿病,近年在減重領域逐漸受到重視。它最關鍵的特性是 – 體重下降來自內臟脂肪與皮下脂肪,而不是肌肉[10]。
這對壓力性肥胖的女性特別有意義,因為皮質醇驅動的,正是「內臟脂肪」的堆積。
更值得注意的是,動物研究顯示 SGLT2 抑制不只是降血糖,還能讓原本紊亂的皮質醇日夜分泌節律,往「比較生理性的型態」回歸 – 這是 GLP-1 類藥物沒有的特性[11]。同時,SGLT2i 對內臟脂肪的抗發炎效果(降低脂肪組織的 IL-6 與 TNF-α),也在壓力性肥胖的「慢性發炎」這條軸線上提供了直接幫助[12]。
Metformin:修復 HPA 軸功能、降低 ACTH 與皮質醇
Metformin 是糖尿病與多囊性卵巢症候群(PCOS)女性熟悉的老藥,但它在壓力性肥胖的角色,過去其實被低估了。
近年研究指出,Metformin 能直接修復飲食誘發肥胖動物模型中失調的 HPA 軸功能、降低 ACTH 與皮質醇分泌[13],並透過 AMPK 路徑改善胰島素敏感度。對「皮質醇主導型」加上「胰島素阻抗」的女性 – 尤其本身就有 PCOS 體質的 – Metformin 的益處往往不只是控糖,而是同時鬆開了「壓力—皮質醇—胰島素」這個三角結構。
換句話說:
- 猛健樂處理的是「想吃的慾望」
- 排糖藥處理的是「皮質醇指定堆積的脂肪 + 慢性發炎」
- Metformin處理的是「胰島素敏感度 – 改善醣類代謝」
對壓力性肥胖的女性,後兩者處理的是病灶端,前者處理的是症狀端 – 這也是為什麼在臨床上,我會更傾向先評估妳真正的失衡型態,再決定藥物的順位與組合,而不是一上來就直接從食慾抑制下手。
當然,這三類藥物都不是所有人都適合,也都有各自需要監測的指標與副作用,任何處方都需要由醫師依個別狀況評估後決定,請勿自行購藥使用。
女性平衡醫學的三條生活修復路徑
藥物可以是工具,但不是地基。對壓力性肥胖,我會優先處理三件事:
1. 重建皮質醇節律,從睡眠下手
固定 11 點前就寢、睡前一小時遠離強光與螢幕、早晨起床立刻接觸自然光 – 這不是「養生建議」,而是真正影響皮質醇日夜節律的生理介入。睡眠剝奪會直接拉高飢餓素(ghrelin)、壓低瘦素(leptin),讓妳隔天無論吃什麼都覺得不夠[7]。
許多女性光是修復睡眠規律,食慾與情緒就會穩定一大半。
2. 抗發炎飲食策略
要讓 GLP-1 受體(不論是內生的,還是猛健樂作用的)真正發揮,必須先降低身體的慢性發炎背景音。
Omega-3(深海魚油)、薑黃素、藍莓綠茶等多酚類食物,都有充分證據支持其抗發炎效果[8]。十字花科蔬菜(花椰菜、甘藍)則能幫助肝臟代謝過剩雌激素,是壓力期女性飲食的基本盤。
3. 對代謝友善的運動,而非高強度對抗
高強度間歇訓練(HIIT)對慢性壓力下的女性不一定是最佳選擇 – 過度的強度本身就是新的壓力源,會進一步刺激皮質醇分泌[9]。
規律步行(每週 150 分鐘)、瑜伽、太極,都能在不加重 HPA 軸負擔的前提下改善胰島素敏感度。對壓力性肥胖的女性,「節奏」比「強度」重要。
找回代謝主導權,從一次完整評估開始
猛健樂不是壞工具,但它是一把「解食慾」的鑰匙,而不是「解壓力」的鑰匙。
在「女性平衡醫學」的觀點裡,每一次減重停滯,其實都是身體在告訴妳:「我這裡還有別的問題沒被看見。」
每個人的失衡狀態不同,壓力性肥胖背後的機制也不盡相同。建議可至初悅診所預約大象醫師的「女性平衡醫學三大系統初步評估」 – 從代謝平衡與內分泌平衡兩個面向,系統性檢視皮質醇節律、慢性發炎指標、胰島素敏感度與荷爾蒙狀態,作為後續個人化調整(包含是否搭配藥物)的判斷基礎。
雖然壓力與肥胖都不是妳的錯,但當它們失去平衡,就會變成讓妳越走越遠的問題。
這也是為什麼我一直在推動「女性平衡醫學」 – 不是等指標崩盤才出手,而是在還來得及的時候,幫妳找回身體該有的節奏。
因為真正重要的,從來不是體重計上的數字,而是妳是否能用一個穩定、自在的身體,去陪伴那些對妳真正重要的事與人。
就從今天開始,先讓身體喘一口氣,再慢慢找回屬於妳的節奏。
參考文獻(References)
- Jastreboff AM, Aronne LJ, Ahmad NN, Wharton S, Connery L, Alves B, Kiyosue A, Zhang S, Liu B, Bunck MC, Stefanski A; SURMOUNT-1 Investigators. Tirzepatide Once Weekly for the Treatment of Obesity. N Engl J Med. 2022 Jul 21;387(3):205–216. doi: 10.1056/NEJMoa2206038. PMID: 35658024.
- Aronne LJ, Sattar N, Horn DB, Bays HE, Wharton S, Lin WY, Ahmad NN, Zhang S, Liao R, Bunck MC, Jouravskaya I, Murphy MA; SURMOUNT-4 Investigators. Continued Treatment With Tirzepatide for Maintenance of Weight Reduction in Adults With Obesity: The SURMOUNT-4 Randomized Clinical Trial. JAMA. 2024 Jan 2;331(1):38–48. doi: 10.1001/jama.2023.24945. PMID: 38078870.
- Kyrou I, Tsigos C. Stress hormones: physiological stress and regulation of metabolism. Curr Opin Pharmacol. 2009 Dec;9(6):787–93. doi: 10.1016/j.coph.2009.08.007. PMID: 19758844.
- Björntorp P. Do stress reactions cause abdominal obesity and comorbidities? Obes Rev. 2001 May;2(2):73–86. doi: 10.1046/j.1467-789x.2001.00027.x. PMID: 12119640.
- Epel ES, McEwen B, Seeman T, Matthews K, Castellazzo G, Brownell KD, Bell J, Ickovics JR. Stress and body shape: stress-induced cortisol secretion is consistently greater among women with central fat. Psychosom Med. 2000 Sep-Oct;62(5):623–32. doi: 10.1097/00006842-200009000-00005. PMID: 11020091.
- Hotamisligil GS. Inflammation, metaflammation and immunometabolic disorders. Nature. 2017 Feb 8;542(7640):177–185. doi: 10.1038/nature21363. PMID: 28179656.
- Spiegel K, Tasali E, Penev P, Van Cauter E. Brief communication: Sleep curtailment in healthy young men is associated with decreased leptin levels, elevated ghrelin levels, and increased hunger and appetite. Ann Intern Med. 2004 Dec 7;141(11):846–50. doi: 10.7326/0003-4819-141-11-200412070-00008. PMID: 15583226.
- Calder PC. Omega-3 fatty acids and inflammatory processes: from molecules to man. Biochem Soc Trans. 2017 Oct 15;45(5):1105–1115. doi: 10.1042/BST20160474. PMID: 28900017.
- Hill EE, Zack E, Battaglini C, Viru M, Viru A, Hackney AC. Exercise and circulating cortisol levels: the intensity threshold effect. J Endocrinol Invest. 2008 Jul;31(7):587–91. doi: 10.1007/BF03345606. PMID: 18787373.
- Pereira MJ, Eriksson JW. Emerging Role of SGLT-2 Inhibitors for the Treatment of Obesity. Drugs. 2019 Feb;79(3):219–230. doi: 10.1007/s40265-019-1057-0. PMID: 30701480.
- Stenvers DJ, Buijs RM, Kalsbeek A, et al. Effects of SGLT2 ablation or inhibition on corticosterone secretion in high-fat-fed mice: exploring a nexus with cytokine levels. Endocrine Connections. 2024;13(8):e240120. doi: 10.1530/EC-24-0120. PMID: 39056197.
- Xu L, Nagata N, Nagashimada M, Zhuge F, Ni Y, Chen G, Mayoux E, Kaneko S, Ota T. SGLT2 Inhibition by Empagliflozin Promotes Fat Utilization and Browning and Attenuates Inflammation and Insulin Resistance by Polarizing M2 Macrophages in Diet-induced Obese Mice. EBioMedicine. 2017 Jun;20:137–149. doi: 10.1016/j.ebiom.2017.05.028. PMID: 28579299.
- Bedard K, Strecko J, Theriault K, Bedard J, Veyrat-Durebex C, Gaudreau P. Effects of a high-glucose diet on the hypothalamic-pituitary-adrenal axis: rescue by metformin. Front Neuroendocrinol. 2021;60:100875. doi: 10.1016/j.yfrne.2020.100875.




